 Всю жизнь работая на электронных микроскопах, я и не подозревал до поры до времени, что отечественная электронная микроскопия создавалась в нашем городе в годы войны. К сожалению, история эта представляет собой одну из неизвестных страниц блокады. Вообще в основе теории электронной микроскопии лежат работы выдающихся физиков конца XIX — начала XX веков. И прежде всего таких, как лауреаты Нобелевской премии Дж. Томсон, открывший в 1898 году электрон, Э. Резерфорд, создатель планетарной модели атома, и Луи де Бройль, установивший в начале 1920-х годов волновую природу электронного пучка и явившийся тем самым основоположником квантовой физики, а также многие другие ученые и инженеры. Их исследования и разработки и позволили создать новый вид микроскопа — электронный, с разрешающей способностью, в 1000 раз превосходящей разрешение самого совершенного светового микроскопа.
Всю жизнь работая на электронных микроскопах, я и не подозревал до поры до времени, что отечественная электронная микроскопия создавалась в нашем городе в годы войны. К сожалению, история эта представляет собой одну из неизвестных страниц блокады. Вообще в основе теории электронной микроскопии лежат работы выдающихся физиков конца XIX — начала XX веков. И прежде всего таких, как лауреаты Нобелевской премии Дж. Томсон, открывший в 1898 году электрон, Э. Резерфорд, создатель планетарной модели атома, и Луи де Бройль, установивший в начале 1920-х годов волновую природу электронного пучка и явившийся тем самым основоположником квантовой физики, а также многие другие ученые и инженеры. Их исследования и разработки и позволили создать новый вид микроскопа — электронный, с разрешающей способностью, в 1000 раз превосходящей разрешение самого совершенного светового микроскопа.
Как писали академики А.И. Опарин и А.Е. Крисс в 1951 году, благодаря использованию электронов, движущихся с большой скоростью, в биологических исследованиях открылась новая эра — эра сверхмикроскопии.
Сами по себе разработка и создание электронного микроскопа (ЭМ) — это величайшее достижение физики и техники XX века и результат целого ряда разнообразных экспериментальных и теоретических исследований, что равносильно научному подвигу. Вдумайтесь в эти факты: уже в 1931 году, то есть менее чем через десятилетие после открытия волновой природы электронов, М. Кноль и Е. Руска в Германии, а затем в 1934 году Л. Мартон в США сконструировали и построили первые ЭМ с магнитными линзами и получили первые изображения.
Мартон вскоре получил и первые электронные микрофотографии биологических объектов. В 1939 году фирма «Сименс — Гальске» в Германии выпустила первую промышленную модель просвечивающего электронного микроскопа, разработанную Б. Боррисом и Е. Руска, а в 1954 году — модернизированный вариант этого ЭМ, широко известный Elmiscop 1…
Ну а что же СССР и советские ученые?
До войны в Советском Союзе теоретические работы по электронной микроскопии проводились в нескольких исследовательских институтах и заводских лабораториях. В 1930-е годы проблему дифракции электронов изучал в Государственном оптическом институте (ГОИ) в Ленинграде А. А. Лебедев, впоследствии академик АН СССР. В 1935 году к нему пришел молодой сотрудник — инженер Виктор Николаевич Верцнер. Он и явился непосредственным разработчиком первого отечественного электронного микроскопа.
Сами работы по проектированию и, как тогда говорили, осуществлению электронного микроскопа начались в 1939 году в руководимой академиком А.А. Лебедевым лаборатории прикладной физической оптики. (Интересно, что слово «осуществление» выражает воплощение некой идеи, а не просто создание технического прибора.) В разработке микроскопа принимал участие также конструктор Н.Г. Зандин, а в испытании и налаживании — научный сотрудник Г.О. Багдыкьянц.
Существовала, между прочим, определенная конкуренция с московскими институтами за право разработки микроскопа нового типа, но предпочтение было все же отдано ГОИ. Курировало и финансировало эти работы Министерство оборонной промышленности. Уже к концу 1940 года была завершена постройка макета первого отечественного принципиально нового ЭМ с электромагнитной оптикой и увеличением до 10.000 раз. Работа над ним не прекращалась даже в тяжелейшие годы войны и блокады, что позволило уже в 1942 — 1943 годах построить вторую, более совершенную, модель электронного микроскопа с увеличением в 25.000 раз, приспособленную для проведения серийных электронно-микроскопических исследований.
Надо сказать, что сам по себе электронный микроскоп — прибор исключительно сложный как в физическом, так и в техническом плане. Работая в тяжелейших условиях блокады, его создатели столкнулись с многими проблемами, в том числе такой, как обеспечение стабилизации высокого напряжения, не говоря уже о точности подгонки всех узлов и деталей. По свидетельству Ю.М. Воронина, нынешнего руководителя лаборатории микроскопии ГОИ, все эти работы производились в корпусах института, расположенных на Васильевском острове рядом с Университетом и Библиотекой Академии наук.
К великому сожалению, сейчас уже нет возможности восстановить в деталях условия и характер сложнейшего труда физиков, техников и рабочих, занимавшихся в годы войны изготовлением ЭМ. Ясно одно, что никакие извинительные причины в расчет тогда не принимались: раз была поставлена задача, то микроскоп должен быть сделан любой ценой. Сейчас эта история кажется невероятной, настолько точной и совершенной должна была быть работа на всех ее этапах. Несомненно, это было подвигом в череде множества подвигов советских людей во время войны.
В 1945 — 1946 годах была разработана и изготовлена уже первая промышленная партия советских электронных микроскопов с увеличением до 100.000 раз. Микроскоп ГОИ, как он тогда назывался, обладал целым рядом технических преимуществ, очевидных для специалистов и остающихся актуальными даже сегодня. В частности, он имел мощный диффузионный насос, позволял получать стереоскопические снимки, а также изучать структуру объектов методом дифракции электронов.
Результаты исследовательской и конструкторской работы над микроскопом были опубликованы В.Н. Верцнером в «Известиях АН СССР» в 1944 году, в журнале «Заводская лаборатория» в 1947 году и в других научных изданиях. Успешная работа над созданием электронного микроскопа позволила академику А.А. Лебедеву отчитаться на общем собрании Академии наук в 1946 году в Москве о постройке первой модели советского электронного микроскопа. Труды разработчиков были по заслугам оценены правительством: в 1947 году А.А. Лебедеву, В.Н. Верцнеру и Н.Г. Зандину была присуждена Сталинская премия.
В дальнейшем работа над созданием промышленных партий отечественных микроскопов новых образцов была поручена Красногорскому оптико-механическому заводу, Сумскому заводу электронных микроскопов (Украина), а также заводу в Выборге, но это уже другая история.
Увы, в последующие мирные, а тем более нынешние рыночные времена деятельность по разработке и созданию новых электронных микроскопов у нас в стране захирела и тихо сошла на нет. Российские заводы не выдержали конкуренции с мощными японскими, немецкими, голландскими и даже чешскими фирмами, поставляющими на рынок совершенные приборы, стоимость которых исчисляется сотнями тысяч долларов. Что касается лаборатории микроскопии ГОИ под руководством Ю.М. Воронина, то она перешла к разработке более компактных зондовых и туннельных электронных микроскопов, использующихся в основном в технике промышленности.
Применительно к биологии электронный микроскоп остается самым сложным, дорогим и совершенным прибором из используемых в этой области знаний. Все имеющиеся на сегодня данные о тонкой морфологической организации животной и растительной клетки, вошедшие в учебники, получены исключительно с помощью электронного микроскопа. Электронная микроскопия и сейчас остается наряду с молекулярной биологией самой передовой отраслью науки о жизни.
Для Зоологического института, где я работаю, электронные микроскопы были закуплены Академией наук в самом начале 1970-х годов, причем уже не отечественные, а зарубежные.
Однако на каких бы приборах мы ни работали, нельзя забывать тех, кто стоял у основ отечественной электронной микроскопии, об их трудах и борьбе. Необходимо также всеми силами поддерживать уже наработанную техническую базу, не дать ей развалиться, уйти в небытие под натиском времени и бездушия. Это нужно прежде всего для нас самих. В этом заключается еще один урок истории.
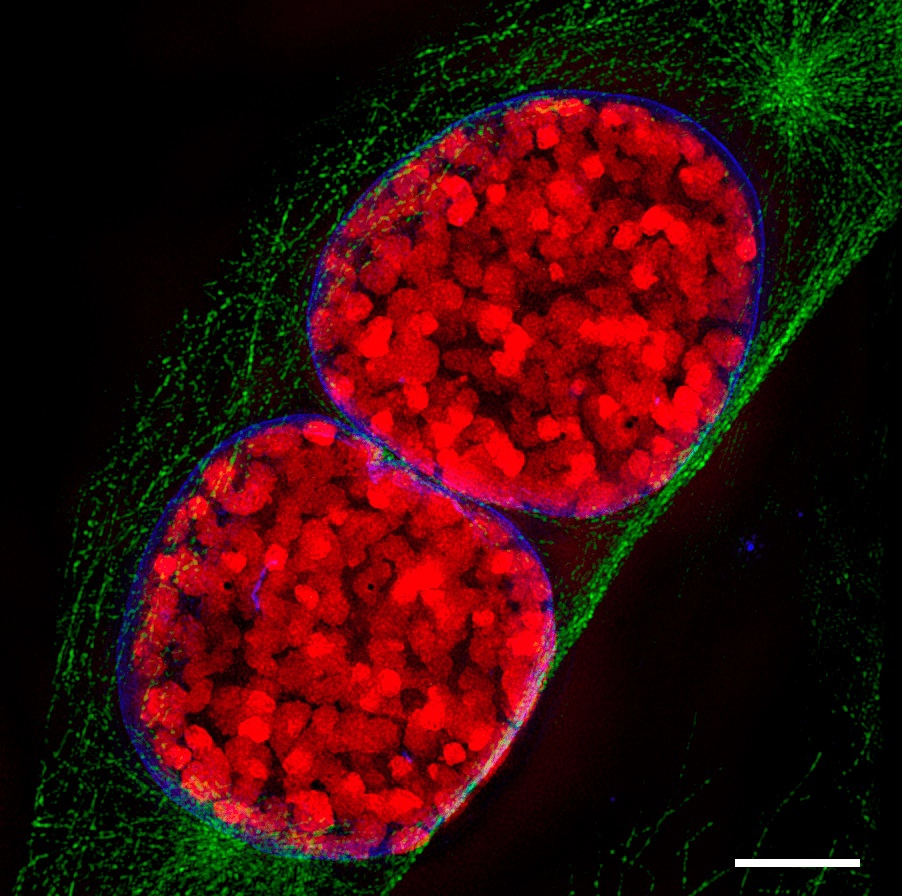
Ни для кого не секрет, что существуют вещи и организмы настолько маленькие, что увидеть их невооруженным глазом просто невозможно. Однако за последние сто лет наука шагнула далеко вперед. И теперь мы можем не только посмотреть на инфузорию, но и увидеть собственными глазами атомы, и даже, буквально, пощупать рельеф микроструктуры кристаллов. А все благодаря электронной микроскопии… Давайте разберемся, как такое возможно.
Перед вами небольшой обзор на электронные микроскопы и их возможности.
 Изображение вируса Эбола, полученное при помощи просвечивающей электронной микроскопии
Изображение вируса Эбола, полученное при помощи просвечивающей электронной микроскопии
Несмотря на то, что «электронная микроскопия» звучит очень современно, запатентована она была еще в 1931 году германо-американским инженером и изобретателем Райнхольдом Руденбергом. Это был настоящий переворот в области изучения микроструктур.
В световом микроскопе, которым на тот момент пользовались исследователи, изображение давали световой луч и незамысловатая конструкция из оптических линз. В электронном микроскопе (ЭМ) роль луча выполнял поток электронов в вакууме, фокусируемый, словно линзами, электромагнитными катушками. Изображение передавалось на флюоресцирующий экран, где его можно было детально рассмотреть. Данная технология позволила исследовать микроструктуры твердых тел, их локальный состав, а также электромагнитные поля.
Как уже было сказано, на исследуемый объект подается пучок электронов, который фокусируется на образце при помощи электромагнитного поля. «Точка» фокусировки электронов имеет не более 5 нм в диаметре. Для сравнения, толщина волоса — 80 000 нм. При соприкосновении с объектом электроны частично проникают внутрь, вытесняя родные электроны и фотоны образца, которые, в свою очередь, попадают на лучевую трубку, где и формируется изображение.
Каковы преимущества электронной микроскопии?
- Первое и основное отличие от светового микроскопа — увеличение. Профессиональный современный световой микроскоп может увеличить изображение в 2 тысячи раз. Электронный микроскоп дает увеличение до 300 тысяч при разрешающей способности 0,5 нм. На таком увеличении уже можно рассмотреть атомы.
- Второе существенное преимущество — при помощи спектрального анализа рентгеновского излучения, возбуждаемого электромагнитным полем, можно изучить химический состав образца в конкретных точках.
- В процессе можно воздействовать на исследуемый объект: облучать, нагревать, намагничивать или деформировать. И полученная картинка будет динамически изменяться.
- Имеется возможность зафиксировать процессы на фото- или видеосъемку в высоком разрешении.
- Исследователь получает электронно-оптическую информацию, которую можно дополнить данными, основанными на дифракции электронов с материалом исследуемого объекта. К примеру, определение показателей кристаллографии при использовании дифракционного контраста.
- В растровой разновидности электронной микроскопии можно рассматривать рельеф поверхности объекта при помощи анализа катодолюминесценции.
А каковы недостатки?
А вот недостатков много:
- Во-первых, в отличие от светового микроскопа, в котором образец можно просто поместить под окуляр, в ЭМ для работы необходим вакуум. Поэтому исследуемые образцы должны быть хорошо обработаны и зафиксированы. А потому невозможно исследовать живые объекты.
- Во-вторых, необходимо сделать ультратонкий срез исследуемого образца: от 20 до 50 нм, который к тому же должен быть равномерным. Иначе электронный поток поглотится объектом и картинки не будет.
- В-третьих, требуется высокое напряжение — от 50 кВ. А вместе с ним и специальная система охлаждения.
- Из-за повышенной чувствительности и хрупкости ЭМ нужно размещать абсолютно неподвижно, на виброустойчивой колонне, в здании без внешних магнитных полей.
- ЭМ создает исключительно черно-белые изображения.
- И, конечно, стоимость. Далеко не каждый исследовательский центр может позволить себе ЭМ. Он дорог и при покупке, и в обслуживании.
Теперь давайте рассмотрим основные виды электронной микроскопии.
А основных видов два:
- Трансмиссионная или просвечивающая электронная микроскопия (ПЭМ)
- Растровая или сканирующая электронная микроскопия (СЭМ)
 Нитчатая водоросоль в световом микроскопе (а), СЭМ (б) и ПЭМ (в)
Нитчатая водоросоль в световом микроскопе (а), СЭМ (б) и ПЭМ (в)
Просвечивающий электронный микроскоп
ПЭМ похож на обычный световой микроскоп, но вместо луча света используется поток электронов, а длина волны намного меньше, чем фотонная. Поэтому изображения получаются в более высоком разрешении.
 Вирус свиного гриппа в просвечивающим электронном микроскопе
Вирус свиного гриппа в просвечивающим электронном микроскопе
Фокусировка электронного потока осуществляется при помощи электромагнитных и электростатических линз. Возникают даже присущие фотонным микроскопам хроматические аберрации. Только природа такого искажения абсолютно иная. Кроме того, за счет закручивания электронов вдоль оси пучка в линзе, возникают дополнительные искажения.
У ПЭМ очень высокое разрешение, что позволяет разглядеть атомы вещества и детально рассмотреть, к примеру, возбудителя вирусного заболевания. Собственно, с появлением полимеразной цепной реакции (ПЦР) и иммуноферментного анализа (ИФА), электронным микроскопом перестали активно пользоваться для определения вирусов. И дело опять в стоимости и трудоемкости..
Из недостатков: объект, помещаемый в ПЭМ, должен быть не толще 1 микрона, то есть как один слой волоса, разрезанного вдоль на 50 частей. А вторая проблема — размер. ПЭМ занимает целую комнату: высотой в человеческий рост и с блоком питания, размером со шкаф.
 Просвечивающий электронный микроскоп
Просвечивающий электронный микроскоп
Сканирующий электронный микроскоп
СЭМ позволяет получать изображение очень высокого разрешения. Узко сфокусированный луч электронов микрон за микроном сканирует поверхность изучаемого образца. СЭМ дает возможность, в том числе, получить трехмерное изображение. У данного типа микроскопов имеется большое количество датчиков, способных улавливать все вытесняемые электронами частицы: электроны, видимый инфракрасный и ультрафиолетовый спектры света, рентгеновское излучение.
В отличие от ПЭМ, работа которого похожа на работу оптического микроскопа, работа СЭМ напоминает устройство старого телевизора. В таких телевизорах есть электронно-лучевая трубка. По ней в вакууме проходят электроны, испускаемые электронной пушкой, и есть система корректирующих движение линз, которые могут фокусировать или отклонять электроны. В СЭМ все то же самое, только электронами обстреливают исследуемый объект, а не люминофоры экрана, а вся поступающая информация фиксируется различными детекторами..
 Сканирующий электронный микроскоп
Сканирующий электронный микроскоп
У СЭМ есть несколько принципиально разных режимов работы, которые зависят от детекторов.
Рассмотрим основные виды:
Детектор вторичных электронов
Используется для определения морфологии поверхности образца, поскольку сигнал вторичных электронов высокочувствителен к рельефу, шероховатостям и неровностям. Чаще всего данный режим работы используется в биологии для определения пор, борозд и изломов, к примеру, при изучении бактериальной клетки.
 Изображение пыльцы, полученное путем детектирования вторичных электронов
Изображение пыльцы, полученное путем детектирования вторичных электронов
Детектор обратно отраженных или обратно рассеянных электронов
Используется для определения состава разносоставного вещества со множеством включений, поскольку сигнал рассеянных электронов чувствителен к специальному композиционному контрасту. Таким образом, на получаемом изображении, вещества разного состава в одном объекте будут иметь разные оттенки серого. Данный режим применяется, в основном, в кристаллографии и биологии.
 Морфология интерфейса между оксидной и металлической составляющими, сделанная в режиме детектирования отраженных электронов
Морфология интерфейса между оксидной и металлической составляющими, сделанная в режиме детектирования отраженных электронов
Энергодисперсионный спектрометр
Позволяет определить элементный состав веществ и включений исследуемого образца. Конечно, в большинстве случаев важнее определить химический, а не элементарный состав. Зато энергодисперсионный спектрометр позволяет точечно, для каждого микрокомпонента определить состав. Кроме того, для данного метода не требуется никаких реагентов. Используется в химии и кристаллографии.
 Анализ элементного состава микрокомпонентов полированного образца анодного шлака с помощью энергодиспрсионного спектрометра
Анализ элементного состава микрокомпонентов полированного образца анодного шлака с помощью энергодиспрсионного спектрометра
Детектор прошедших электронов
Электроны, прошедшие тонкий срез образца насквозь, приходят к датчику под разным углом, что дает различную информацию об исследуемом объекте. Угол рассеивания зависит от толщины среза, материала образца и энергии первичного электронного пучка. Детектор передает псевдоцветное изображение, где каждый цвет соответствует своему сигналу.
 Коррозия, распространяющаяся сквозь хромовое покрытие на стали. Изображение получено при помощи детектирования прошедших электронов.
Коррозия, распространяющаяся сквозь хромовое покрытие на стали. Изображение получено при помощи детектирования прошедших электронов.
Детектор катодолюминесцентного излучения
Используется при изучении материалов, обладающих люминесценцией, то есть способные излучать видимый свет при попадании на них электронного потока.
Катодолюминесценция — это, по сути, способность вещества замещать оставленные после облучения электронами дырки, захватывая свободные электроны и выделяя световую энергию. Это свойственно для металлов: чистых и с примесями. Свет, производимый металлом с примесью, будет другого оттенка, что и будет фиксироваться детектором..
 Изображение циркона, полученное при детектировании катодолюминесцентного излучения
Изображение циркона, полученное при детектировании катодолюминесцентного излучения
СЭМ может работать исключительно с твердыми образцами в вакууме. Поэтому для работы с жидкостями, их необходимо подвергнуть глубокой заморозке. Зато форма и размер образца могут быть любыми в пределах объема рабочей камеры. Продуктивность работы повышается при нанесении на исследуемый образец тонкого слоя токопроводящего материала.
Электронная микроскопия применяется во многих сферах науки и промышленности:
Биология и медицина
При помощи ЭМ можно осуществить томографию тканей, детально рассмотреть клетки, определить локализацию белков, увидеть вирус и даже выполнить фармацевтический контроль качества.
Физика, химия и кристаллография.
ЭМ позволяет изучить микроструктуры металлов и кристаллов вещества, классифицировать материалы, тестировать характеристики различных веществ, определять состав, поверхность и плотность объектов.
Полупроводники и хранение данных
С помощью ЭМ выявляются и редактируются неисправности систем, выполняется анализ дефектов.
Промышленность
ЭМ помогает определять параметры частиц и целых структур. Позволяет в динамике посмотреть на материалы в высоком разрешении. При необходимости дает возможность построения трехмерной модели микроструктуры.
В некоторых сферах электронная микроскопия незаменима. Поэтому исследователи постоянно работают над усовершенствованием методов и возможностей в данной области. Рассмотрим некоторые из них.
В некоторых случаях, к примеру, в биологии и медицине, могут потребоваться не просто фотографии ультратонких срезов, а трехмерные изображения какой-либо ткани или организма.
Это возможно осуществить несколькими способами:
1. ПЭМ серийных срезов
2. Криоэлектронная томография
По сравнению с ПЭМ серийных срезов, позволяет увидеть в более высоком разрешении более мелкие структуры, величиной от 3 нм, к примеру, элементы цитоскелета. Однако образцы должны быть довольно мелкими (100—500 нм) поэтому КЭТ не применима для крупных объектов и подходит только для молекулярных комплексов, вирусов и мелких бактерий.
 Принцип метода криоэлектронной томографии
Принцип метода криоэлектронной томографии
В процессе КЭТ объект исследования постепенно поворачивается и изображения получаются под разным углом наклона. После этого все фотографии сводятся в одно 3D изображение. Минус метода в том, что образец получает высокую дозу излучения, за счет чего часть мелких деталей теряется в процессе исследования.
3. Многоэнергетическая деконволюция
4. Фокусирующая ионно-лучевая сканирующая электронная микроскопия (ФИЛ-СЭМ)
Суть метода заключается в параллельном «разрезании» исследуемого образца на слои пучком ионов галлия и сканировании объекта электронным пучком. Слой получается толщиной 5—10 нм. Полученные изображения собираются в единую трехмерную модель.
 Раскрашенное изображение бактериофагов (зеленые), поразивших кишечную палочку (голубые), сделанное в ФИЛ-СЭМ
Раскрашенное изображение бактериофагов (зеленые), поразивших кишечную палочку (голубые), сделанное в ФИЛ-СЭМ
Сложность метода в подготовке. Перед проведением операции необходимо защитить образец от части заряда. Для этого на сам объект, к примеру, кусок органа, напыляется металл, а блок, в который заключен образец, покрывается серебряной пастой. Максимальный размер моделируемого объекта — 100*100 мкм. Кроме того, метод очень долгий, а с увеличением глубины резки снижается качество.
 Принцип метода ФИЛ-СЭМ
Принцип метода ФИЛ-СЭМ
5. СЭМ с автоматизированной лентой для сбора срезов
По сути, это улучшенная версия метода серийных срезов. Специальная насадка на ультрамикротом, который делает срезы, работает автоматически и способна делать до 1000 срезов в день, помещая их на специальную ленту. Далее лента разрезается на фрагменты, кладется на подложку, срезы обрабатываются контрастом и углеродом, после чего разрезанный образец помещается в СЭМ. Полученные изображения имеют разрешение 5 нм.
 Ультрамикротом со специальной насадкой и вставленной лентой для срезов
Ультрамикротом со специальной насадкой и вставленной лентой для срезов
6. Последовательная сканирующая электронная микроскопия поверхности блока
Используется для получения трехмерной модели большого объекта. Для этого ультрамикротом помещается внутрь СЭМ. В процессе происходит последовательное срезание ультратонких слоев образца с последующим сканированием. Для улучшения изображения может использоваться контраст. Преимущество данного метода заключается в величине объекта и скорости обработки информации. За получаемыми данными можно наблюдать в реальном времени.
Цветное изображение
Большим минусом ЭМ является черно-белое изображение. Однако и с этим ученые смогли справиться.
Самый простой метод — коррелятивная свето-электронная микроскопия (КСЭМ). Для окрашивания изображения один и тот же объект фотографируется в световом и в электронном микроскопе, а затем программа соединяет два изображения. Однако из-за разницы в разрешении изображение лишь радужно подкрашивается согласно распределению флуоресцентного красителя. Выделить микроструктуры таким образом не удастся.
 Коррелятивная свето-электронная микроскопия элементов цитоскелета
Коррелятивная свето-электронная микроскопия элементов цитоскелета
Ученые объединили КСЭМ с трехмерной световой микроскопией, уже известной нам ФИЛ-СЭМ и с микроскопией сверхвысокого разрешения (СР-микроскопия), которая позволяет получить большее разрешение за счет объединения на экране множества снимков.
 Срез ядер нейронов при микроскопии сверхвысокого разрешения
Срез ядер нейронов при микроскопии сверхвысокого разрешения
Составив изначально изображение высокого разрешения, ученые резали образец лучами ионов. Изображение получало цвет за счет световой микроскопии структурированного освещения, позволяющего увеличить разрешение снимка в два раза за счет поочередной подсветки отдельных точек при фоновом свечении остального образца, и одномолекулярной световой микроскопии, при которой флуоресценция красителя активируется слабым лазером. Одномолекулярная микроскопия позволяет получить изображение с разрешением 0,2 мкм. Все полученные изображения свели вместе и получили полноценные цветные снимки. С помощью данной методики удалось разглядеть, к примеру, ультраструктуру нейронов.
 Трехмерные модели ядер нейронов, полученные при коррелятивной микроскопии
Трехмерные модели ядер нейронов, полученные при коррелятивной микроскопии
Итак, электронный микроскоп — вещь, во многих сферах незаменимая. Ученые потихоньку нивелируют его минусы и решают проблемы, связанные с его использованием. Возможно, в скором времени, из минусов останутся только размер и стоимость. Хотя… Может, и это исправимо?
Использованная литература:
- Гоулдстейн Дж., Ньюбери Д., Эчлин П., Джой Д., Фиори Ч., Лифшин Ф. Растровая электронная микроскопия и рентгеновский микроанализ: в двух книгах. Пер. с англ. — М.: Мир, 1984. 303 с.
- Уманский Я. С., Скаков Ю. А., Иванов А. Н., Расторгуев Л. Н… Кристаллография, рентгенография и электронная микроскопия. — М.: Металлургия, 1982, 632 с.
- СиндоД. Оикава. Т. Аналитическая просвечивающая электронная микроскопия. — М.: Техносфера, 2006, 256 с. ISBN 5-94836-064-4.
- Denk, W., & Horstmann, H. (2004). Serial block-face scanning electron microscopy to reconstruct three-dimensional tissue nanostructure. PLoS Biology, 2(11).
- Efimov, A. E., Tonevitsky, A. G., Dittrich, M., & Matsko, N. B. (2007). Atomic force microscope (AFM) combined with the ultramicrotome: A novel device for the serial section tomography and AFM/TEM complementary structural analysis of biological and polymer samples. Journal of Microscopy, 226(3), 207–217. doi.org/10.1111/j.1365-2818.2007.01773.x
- Peddie, C. J., & Collinson, L. M. (2014). Exploring the third dimension: Volume electron microscopy comes of age. Micron. Elsevier Ltd. doi.org/10.1016/j.micron.2014.01.009
- Schalek, R., Kasthuri, N., Hayworth, K., Berger, D., Tapia, J., Morgan, J., … Lichtman, J. (2011). Development of High-Throughput, High-Resolution 3D Reconstruction of Large-Volume Biological Tissue Using Automated Tape Collection Ultramicrotomy and Scanning Electron Microscopy. Microscopy and Microanalysis, 17(S2), 966–967. doi.org/10.1017/S1431927611005708
- Wagner, J., Schaffer, M., & Fernández-Busnadiego, R. (2017, September 1). Cryo-electron tomography—the cell biology that came in from the cold. FEBS Letters. Wiley Blackwell. doi.org/10.1002/1873-3468.12757
- https://biomolecula.ru/articles/po-tu-storonu-difraktsionnogo-barera-nobelevskaia-premiia-po-khimii-2014
- https://biomolecula.ru/articles/fluorestsiruiushchaia-nobelevskaia-premiia-po-khimii
- https://biomolecula.ru/articles/tsvet-3d-i-sverkhvysokoe-razreshenie-novaia-razrabotka-v-mikroskopii
Источники: https://habr.com/, https://www.infran.ru/
Авторы: Биореактор @InBioReactor, Андрей ШАТРОВ, Соловьёва Софья

